更新日:2020年7月16日
再生医療等の安全性の確保等
再生医療等の安全性の確保等に関する法律等(医薬品医療機器等法に該当するものを除く)
- 関係法令等は、再生医療について(厚生労働省ホームページ)をご覧ください。
- 認定再生医療等委員会、特定細胞加工物製造事業者及び再生医療等提供計画等の申請、届出は、「各種申請書作成支援サイト(外部サイト)」をご利用ください。
※(参考)申請、届出の際は、Q&A・記載要領等(厚生労働省ホームページ)、よくあるご質問も、あわせてご覧ください。
定期報告
再生医療等提供機関及び特定細胞加工物製造事業者は、1年毎に定期報告を提出する必要があります。
※定期報告カレンダーを作成しましたので、今後の定期報告の提出期限の確認等にご活用ください。
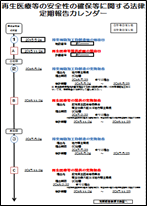
カレンダー使用方法
特定細胞加工物製造事業者
施設番号を入力してください(F10セル)。
→自動的に2年目以降の日付が表示されます。
再生医療等提供機関
計画番号を入力してください(F13セル)。
→自動的に2年目以降の日付が表示されます。
お問い合わせ窓口
ご不明点等ございましたら、下記までお願いします。
北海道厚生局 健康福祉部 医事課 再生医療等推進係
- 住所
- 〒060-0808 北海道札幌市北区北8条西2丁目1番1号 札幌第1合同庁舎8階
- 電話
- 011-709-2311(内線3945)
- メール
- hsaiseiiryou♦mhlw.go.jp
※迷惑メール防止のため、メールアドレスの一部を変えています。「♦」を「@」に置き換えて下さい。
※メール送信の際には、「1.機関名 2.所在地 3.電話番号 4.担当者名 5.相談内容」を明記の上、お問い合わせ下さい。


